Ученые РМАНПО приняли участие в создании первого фармакогенетического атласа России
Коллектив фармакогенетиков Российской медицинской академии непрерывного профессионального образования под руководством член-корреспондента РАН Д.А. Сычева в сотрудничестве с двумя коллективами популяционных генетиков1 (под руководством профессора Е.В. Балановской и профессора РАН О.П. Балановского) создал первую рабочую версию фармакогенетического атласа России – систематического собрания геногеографических карт распространенности фармакогенетических ДНК маркеров по всей территории России и сопредельных стран.
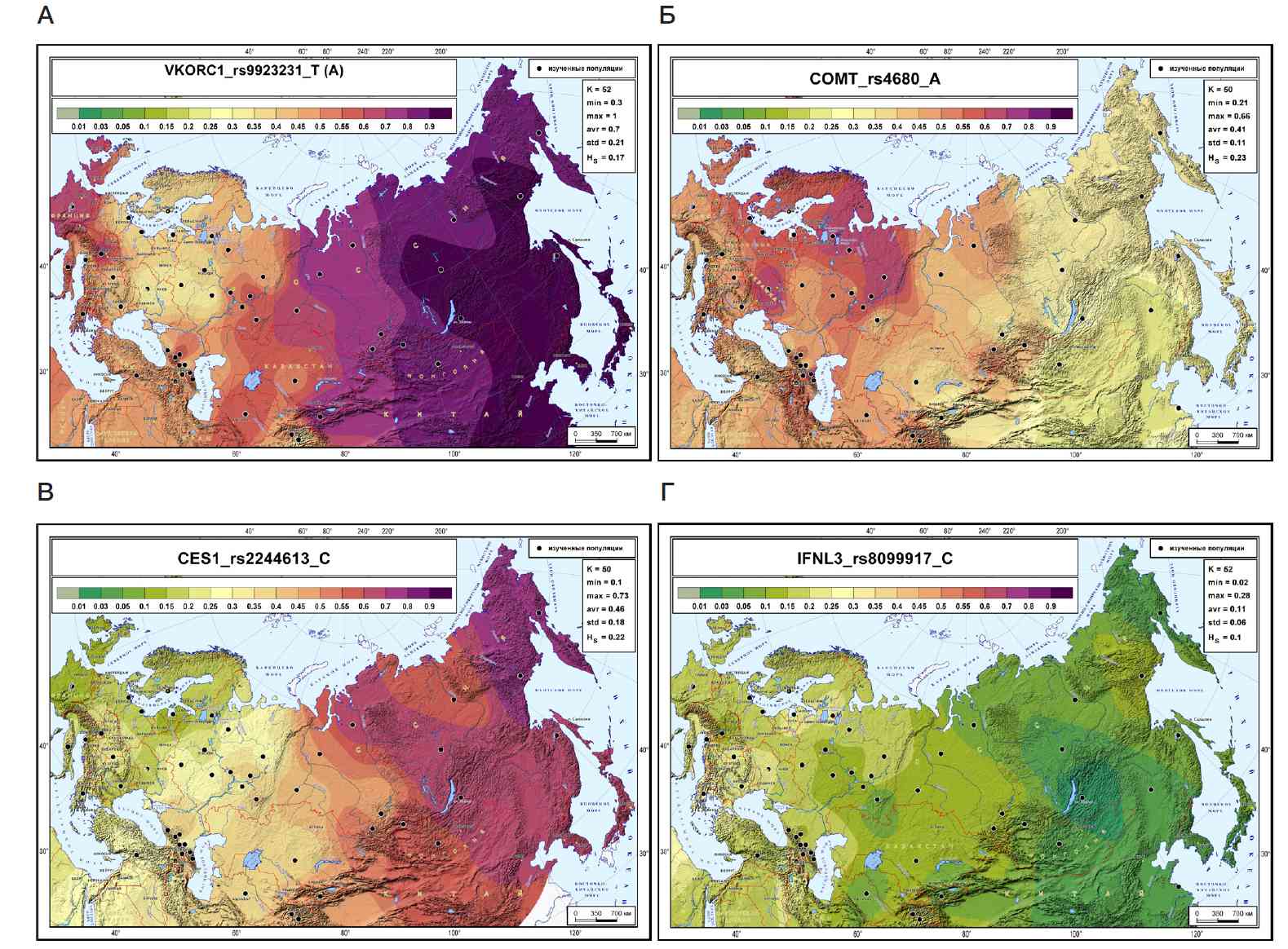
Карты распределения частот фармакогенетических маркеров с паттерном клинальной пространственной изменчивости: VKORC1 (rs9923231-T(A)) (А); COMT (rs4680-A) (Б); CES1 (rs2244613-C) (В); IFNL3 (rs8099917-C) (Г)
Атлас состоит из 45 карт частот генетических вариантов, признанных важными в фармакогенетике и персонализированной медицине. Карты показывают распространение этих ДНК-маркеров в 50 популяциях, охватывающих 137 этнических и субэтнических групп населения Российской Федерации и сопредельных государств. Карты атласа выявили три основных паттерна изменчивости: клинальная изменчивость по оси «восток-запад», равномерное распределение и очаговая изменчивость.Необходимость создания атласа обоснована тем, что действие лекарств на разных людей не одинаково, поскольку зависит от работы большого количества генов, изучением которых занимается фармакогенетика. Она лежит в основе персонализированного подхода к лечению: разрабатываются клинические протоколы подбора препарата и его дозы в зависимости от генотипа данного пациента. Фармакогенетический анализ может быть проведен не только для индивида, но и для популяции в целом: в этом случае учитывается усредненный генотип, основанный на частотах аллелей в популяции. Разумеется, индивидуальные генотипы могут отличаться от средних показателей популяции. Тем не менее, усредненный прогноз для популяции, учитывающий особенности ее генофонда, лучше подходит для ее членов, чем стандартные рекомендации по выбору препаратов и их дозировок. Поэтому, если нет возможности провести дорогостоящее исследование генотипа пациента, можно ориентироваться на частоту ДНК маркеров в том этногеографическом регионе, из которого происходит пациент и его предки.
Рабочая версия атласа фармакогенетических маркеров будет дополняться и совершенствоваться. Данные о распространенности клинически значимых генетических вариантов в российских популяциях должны помочь внедрению разработанных фармакогенетических алгоритмов на территории нашей страны. Таким образом, это важный шаг в направлении персонализированной медицины будущего.
Подробнее о работе: генофонд.рф
Ознакомиться с полным текстом статьи: https://vestnik.rsmu.press/archive/2020/6/12/abstract?lang=ru